江西专业的HE染色报告
HE染色构成组织内蛋白质的氨基酸的种类很多,它们有不同的等电点。在普通染色法中,染色液的酸碱度为pH6左右,细胞内的酸性物质如细胞核的染色质、腺细胞和神经细胞内的粗面内质网及透明软骨基质等均被碱性染料染色,这些物质称为嗜碱性。而细胞质中的其它蛋白质如红细胞中的血红蛋白、嗜酸粒细胞的颗粒及胶原纤维和肌纤维等被酸性染料染色,这些物质称为嗜酸型。如果改变染色液的酸碱度,pH值升高时,则原来被酸性染料染色的物质可变为嗜碱性;pH值降低时,原来被碱性染料染色的物质则可变为嗜酸性。所以说染色液的pH值可以影响染色的反应。HE染色原理 试剂 染色步骤 注意事项 。江西专业的HE染色报告

HE染色多聚甲醛保存组织的注意事项:多聚甲醛放置过久其中的醛基可能会被氧化为酸,使溶液pH降低,从而影响染色。不同细胞或组织样品所需的固定时间有所不同,应当根据细胞或组织的种类以及组织块的大小来调整固定时间。多聚甲醛虽然作用温和,但能硬化组织,固定时间过久会导致组织变脆,切片时易碎。因此固定时间通常不宜超过24小时。多聚甲醛可长期存在于固定过的细胞或组织样品中,固定完成后用适当的洗涤液或水冲洗数小时仍会有残留,因此后续实验结果如果受醛基影响,须尽量洗去残留的多聚甲醛。醛基与抗原蛋白的氨基交联形成羧甲基,使抗原决定簇的三维构象出现空间障碍。分子间交联形成的网格结构可能部分或完全掩盖某些抗原决定簇,使之不能充分暴露,可造成假阴性的染色,影响免疫组化结果。因此,4%多聚甲醛固定的细胞或组织样品在进行免疫组化检测时,有时需要对抗原先进行修复,然后才能进行免疫染色等后续操作。山东比较好的HE染色价格HE染色是组织学、病理学教学与科研中比较基础、使用比较普遍的技术方法之一。
HE染色组织样本水化:将浸泡过二甲苯的待测组织样本先放入无水乙醇中浸泡5min,使脱蜡时用的二甲苯可以被洗脱出去,使水可以进入组织中;再依次置于95%、85%、70%乙醇中各浸泡5min以达到充分水化的效果。组织切片苏木素染色、分化与反蓝:将水化后的组织样本的切片使用PBS溶液浸泡清洗,每次浸泡5min,总共清洗3次。之后用移液***吸取已经预先配制好的苏木素染色液,每个组织切片滴加100ul,充分染色10min。染色完毕后使用蒸馏水洗去多余的苏木素染色液。然后再使用1%的盐酸乙醇进行分化,使细胞核中结合过多的染液和细胞浆中的多余的染液被除去。分化完成后,再用双蒸水将组织切片冲洗干净。为了使苏木素染蓝色,使用弱碱性的促蓝液加入组织切片中,让细胞核染蓝色。反蓝结束后先用清水进行清洗,再用双蒸水将组织切片冲洗干净。
HE染色切片中出现类似色素样的点状结晶和黑色光滑的细胞核原因:切片封片前放置在空气中时间太长,以至于二甲苯挥发切片干燥所致。对策:移去组织切片上的盖玻片和封固剂,重新处理。将切片水洗数分钟,然后重新脱水、透明、封固。封片过程中要保持组织切片的轻度湿润,尽量不要让其干燥。细胞核呈红、棕色改变原因:苏木精染色液过度氧化和切片在苏木精染液染色后返蓝不足。对策:首先,每次染色之前检查苏木精染色液的染色能力,发现氧化过度应及时更换。其次,可用流水、温水或弱碱性溶液如稀氨水、0.2%碳酸氢钠等,在苏木精染色后,给切片以足够的蓝化时间。HE染色,优先南京英瀚斯生物。
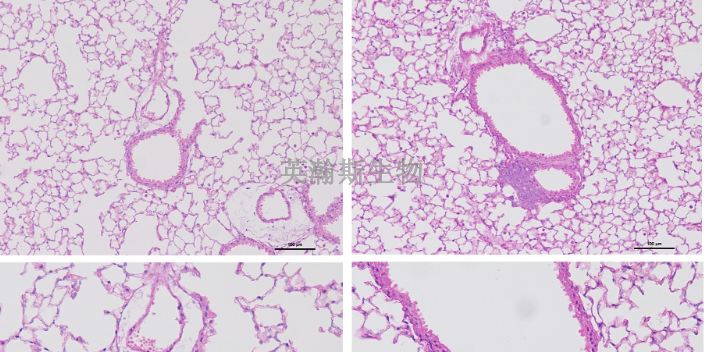
HE染色常见问题:Q5:细胞核呈棕红色改变答:苏木素染液过度氧化;或苏木素染色后反蓝不足导致。应该立即更换苏木素染色液。或在流动自来水(一般自来水PH7.5-7.8),或在稀释的氨水溶液,或在0.2%碳酸氢钠中适当浸泡,这些步骤均可一定程度地加强苏木素染色后的反蓝效果。Q6:伊红染色较淡答:伊红的PH改变了(PH可能已大于5);或反蓝液体未漂洗干净,残留后影响胞浆嗜酸性染色;或者切片太薄并且在随后的脱水步骤停留过久。对策:检查伊红染色液PH,可采用乙酸调至4.6-5.0。根据以上提示,调整实验步骤。冰冻切片是否可以做HE染色?海南结果客观的HE染色报告
科研常备实验操作之HE染色。江西专业的HE染色报告
HE染色碱染料染主要使细胞核内的染色质与胞质内的核糖体着色。学上常用的一种染色方法为苏木精 伊红染色法。苏木精 伊红染色法 ( hematoxylin-eosin staining ) ,简称HE染色法 ,石蜡切片技术里常用的染色法之一 。苏木精染液为碱 ,主要使细胞核内的染色质与胞质内的核糖体着紫蓝色 ;伊红为酸染料 ,主要使细胞质和细胞外基质中的成分着红色 。细胞核被苏木精染成鲜明的蓝色,软骨基质、钙盐颗粒呈深蓝色,粘液呈灰蓝色。细胞浆被伊红染成深浅不同的粉红色至桃红色,胞浆内嗜酸颗粒呈强的鲜红色。胶原纤维呈淡粉红色,力纤维呈亮粉红色,红血球呈橘红色,蛋白液体呈粉红色。江西专业的HE染色报告
- 江苏结果客观的HE染色报告 2025-07-30
- 海南靠谱的HE染色多少钱 2025-07-30
- 福建肺纤维化模型如何构建 2025-07-29
- 重庆病理HE染色多少钱 2025-07-29
- 江苏推荐的HE染色多少钱 2025-07-29
- 吉林比较好的HE染色外包 2025-07-29
- 黑龙江结果客观的HE染色报告 2025-07-29
- 湖北病理HE染色报告 2025-07-29
- 天津HE染色公司 2025-07-29
- 四川结果客观的HE染色报告 2025-07-29
- 杭州流式细胞仪品牌 2025-07-30
- 自主研发足底压力板 2025-07-30
- 台州内窥镜模组供应商 2025-07-30
- 三联吡啶氯化钌六水合物现货 2025-07-30
- 江苏进口胎牛血清批发厂家 2025-07-30
- 苏州一次性CGT配件耗材ODM服务 2025-07-30
- 崇明区质量鼻氧管销售方法 2025-07-30
- 嘉定区叶绿素荧光成像系统产品 2025-07-30
- 济南密封性研究微生物检测价格 2025-07-30
- 普陀区作用内窥镜专卖店 2025-07-30