吉林比较好的肺纤维化模型如何构建
在肺纤维化模型中,肺组织经历了一个复杂而微妙的转变过程,即从炎症逐渐过渡到纤维化。这个过程模拟了人类肺部在遭受长期炎症损伤后,如何逐渐失去其原有的弹性和功能,转而形成坚硬的纤维组织。炎症阶段,肺组织中的免疫细胞被激发,释放出各种炎症介质,导致肺组织受损。随着时间的推移,这些炎症损伤无法得到有效修复,肺组织开始尝试通过纤维化来自我修复,然而这一过程却导致了肺组织的进一步硬化和功能障碍。肺纤维化模型不仅为我们揭示了这一转变的详细过程,也为深入研究肺纤维化的发病机制和治疗方法提供了重要依据。肺纤维化模型有助于理解肺纤维化对患者心理健康和生活质量的影响。吉林比较好的肺纤维化模型如何构建
在肺纤维化模型中,胶原蛋白的过度沉积是一个明显且重要的特征,它直接关联着肺纤维化的病理过程。在正常情况下,胶原蛋白是维持肺部结构稳定的重要成分,但在肺纤维化的情况下,由于炎症的持续刺激和修复机制的异常,导致胶原蛋白的生成与降解失衡。在肺纤维化模型中,可以清晰地观察到,随着疾病的进展,肺泡壁和肺间质中胶原蛋白的沉积逐渐增加,这些沉积的胶原蛋白会逐渐形成纤维束,使肺组织变得僵硬,失去原有的弹性。这种胶原蛋白的过度沉积不仅影响了肺部的正常功能,还是肺纤维化疾病的重要标志之一。陕西肺纤维化模型有哪家肺纤维化模型有助于评估肺纤维化疗愈对患者生活质量的影响。
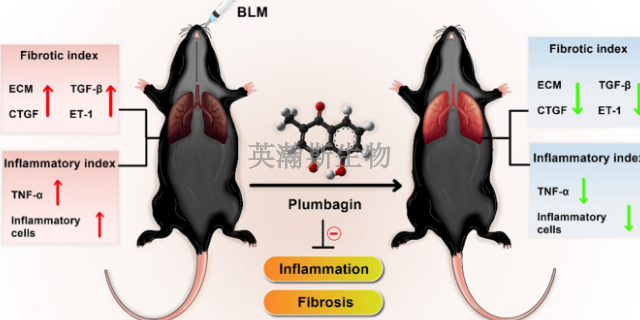
肺纤维化模型的病理特点为肺部炎症引起肺泡反复持续性损伤及细胞外基质的破坏、修复和过度沉积。该病严重影响患者生存质量,预后极差。由于该病发病机制到目前为止尚不清楚,临床上也缺乏相应的有效疗愈手段,患者病死率居高不下,因此建立一个可靠稳定的肺纤维化动物模型是探索其发病机制和开发有效疗愈药物的重要前提,实验中常用的肺纤维化诱导剂主要有博莱霉素、***、二氧化硅、石棉、放射线、呼肠病毒、野百合碱等,在这些诱导剂中,以博莱霉素使用比较为普遍,己成为经典的动物肺纤维化模型的诱导剂。
肺纤维化模型在肺纤维化研究领域中具有不可替代的地位,其中尤为突出的是它为研究肺纤维化的遗传因素提供了极大的便利。遗传因素在肺纤维化的发病过程中扮演着重要角色,不同的基因变异可能导致个体对肺纤维化的易感性增加。通过肺纤维化模型,研究人员能够模拟不同基因背景下的肺纤维化过程,从而深入探讨特定基因变异对疾病进程的影响。这种模型的应用使得研究人员能够在实验室中模拟出类似于人类的遗传背景,进而研究遗传因素在肺纤维化中的作用机制。这不仅有助于揭示肺纤维化的遗传基础,还为基于遗传学的疗愈策略的开发提供了重要的理论支持。肺纤维化模型为研究肺纤维化的遗传因素提供了便利。
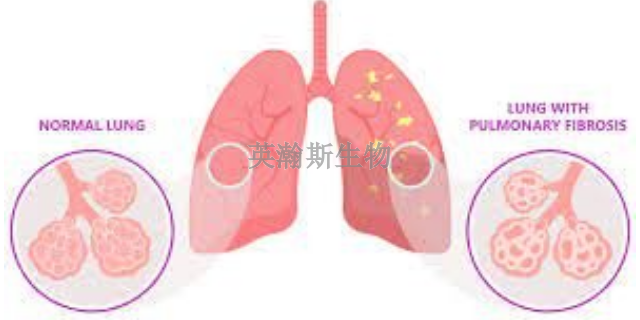
许多物质和疾病都可以导致肺纤维化。即便如此,在很多情况下无法找到具体原因。不明原因的肺纤维化叫做特发性肺纤维化。研究人员对引发特发性肺纤维化的原因有几种理论,包括病毒和接触***烟雾。此外,一些形式的特发性肺纤维化在家族中遗传,遗传可能在特发性肺纤维化中发挥作用。许多特发性肺纤维化患者也可能患有胃食管反流病(GERD)—一种胃酸流回食管的疾病。目前已有研究在评估GERD是否可能是导致特发性肺纤维化的风险因素,或者GERD是否可能导致病情进展更快。但还需要开展更多的研究来确定特发性肺纤维化与GERD之间的联系。在肺纤维化模型中,肺组织经历了从炎症到纤维化的转变。宁夏推荐的肺纤维化模型有哪些
肺纤维化模型有助于评估不同药物在肺纤维化疗愈中的安全性。吉林比较好的肺纤维化模型如何构建
肺纤维化模型发展时间:给药后第 7 天肺组织大多呈重度肺泡炎改变,肺泡腔及肺间质内有大量中性粒细胞浸润,部分肺泡腔破坏或消失,肺间隔内成纤维细胞和***增生,与正常肺组织对比差别明显;给药后第14天,肺纤维化开始形成。巨噬细胞、中性粒细胞等炎性细胞明显减少,成纤维细胞增多,肺泡间隔明显增厚,有胶原沉积。给药后第28天,多数小鼠发生弥漫性肺间质纤维化,肺间质被胶原纤维和成纤维细胞替代,肺泡壁破坏,肺大泡形成,但仍可见炎性细胞浸润。吉林比较好的肺纤维化模型如何构建
- 四川小鼠肺纤维化模型怎么造模 2025-07-17
- 专门做肺纤维化模型 2025-07-17
- 宁夏靠谱的肺纤维化模型动物实验外包 2025-07-17
- 甘肃大鼠肺纤维化模型是哪家 2025-07-17
- 广西哪里有肺纤维化模型动物实验外包 2025-07-17
- 海南大鼠肺纤维化模型有哪些 2025-07-17
- 吉林比较好的肺纤维化模型如何构建 2025-07-16
- 湖北肺纤维化模型动物实验外包 2025-07-16
- 宁夏推荐的肺纤维化模型有哪些 2025-07-16
- 河南大鼠肺纤维化模型有哪家 2025-07-16
- 福建数字化手术直播会诊平台厂家 2025-07-17
- 南京运用分子耗材 2025-07-17
- 上海虚实结合虚拟仿真多少钱 2025-07-17
- 惠州大号医疗舱售后服务 2025-07-17
- 宁夏全自动艾灸机器人 2025-07-17
- 湖北效果好的地巾布巾清洗消毒机使用方法 2025-07-17
- 河北成人鼻腔喷雾品牌排行 2025-07-17
- 浦东新区本地生物检测试剂盒 2025-07-17
- 深圳特色菌群移植供体 2025-07-17
- 西北自凝牙托粉 2025-07-17