化学膜片钳技术原理
化学膜片钳技术在生物医学研究中展现出多方面的明显优势。首先,它能够直接记录细胞膜上离子通道的电流变化,具有极高的灵敏度和时间分辨率,可以捕捉到单通道电流的微小变化。这种高灵敏度使得研究人员能够在细胞水平上观察到离子通道的开闭状态以及电流的动态变化,为深入理解细胞膜的电生理特性提供了有力支持。其次,该技术通过高阻封接实现对细胞膜的电学隔离,背景噪声低,能够准确测量离子通道的活动。这种低噪声特性确保了测量结果的可靠性,避免了因外界干扰而产生的误判。光遗传技术作为一种新兴的生物技术,正处于快速发展阶段。化学膜片钳技术原理
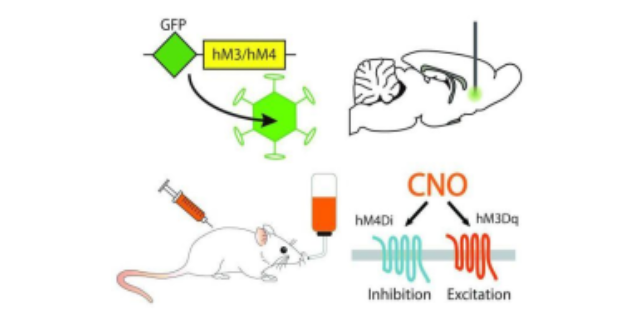
光遗传学技术在药物研发方面有哪些应用?疼痛管理在疼痛管理中,光遗传学展现出其独特的应用价值.研究人员可以通过光遗传学技术打开或抑制与疼痛相关的神经元,从而实现对疼痛的有效控制.这种非侵入性的疼痛管理方式,为开发新的镇痛药物提供了新的思路.在瘤治中,光遗传学技术提供了一种全新的策略.利用光敏蛋白,科学家们可以在瘤子细胞中诱导选择性细胞死亡,从而实现对瘤子的精确治着.这种治着方法不只具有高度特异性,而且能够减少对正常细胞的损伤,有望降低治着过程中的副作用.化学膜片钳技术原理光遗传学技术结合光学与遗传学手段,能够精确控制特定神经元活动。
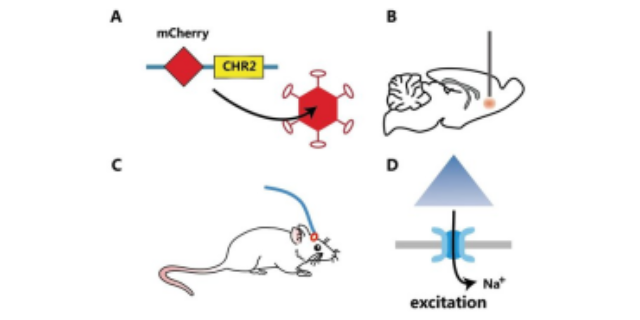
光遗传化学遗传技术对于精神疾病医疗,光遗传化学遗传技术带来了新希望。以抑郁症为例,研究发现大脑中某些神经环路的活动异常与抑郁症状相关。通过将光遗传工具或 DREADD 受体导入这些神经环路的神经元,在动物模型中,利用光或配体调控神经活动,改善抑郁样行为。未来有望将这种技术转化为临床医疗手段,例如通过植入式光刺激装置或可控的配体给药系统,精细调节患者大脑中异常的神经环路,为传统医疗效果不佳的精神疾病患者提供新的医疗选择。
在化学遗传技术中,设计和合成具有特异性的受体是关键环节。以 DREADD 技术为例,研究人员通过对天然 G 蛋白偶联受体(GPCR)进行结构改造,引入特定的氨基酸突变,使其失去对天然配体的响应能力,同时获得对人工合成化合物的高度特异性结合能力。这些改造后的受体在细胞表面表达后,能够精细地识别并结合相应的化学小分子,从而实现对细胞内信号通路的特异性调控。受体的设计需要深入了解 GPCR 的结构与功能关系,以及化学小分子与受体的相互作用机制。同时,化学小分子的合成也需要精细的有机化学合成方法,确保其纯度和活性。通过不断优化受体和化学小分子的设计与合成,化学遗传技术能够实现对细胞功能更精细、更高效的调控,为研究复杂的生物系统提供了有力手段。如何将光遗传学技术应用到临床实践中,也需要更多的研究和探索。
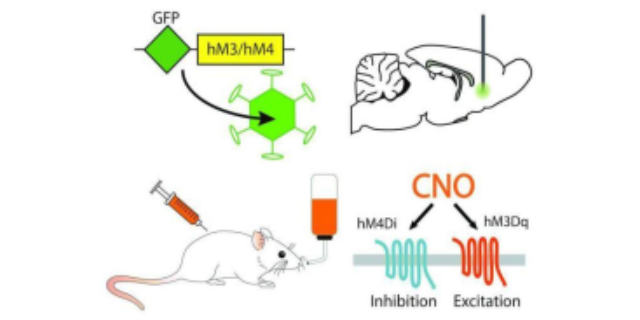
化学遗传技术方案与传统生物技术存在明显差异,其突出特点在于化学工具的引入打破了生物研究的固有边界。传统基因敲除、过表达技术依赖于基因工程手段,往往需要较长时间构建模型且难以实现对蛋白功能的瞬时调控。而化学遗传技术凭借小分子化合物的快速渗透和高效结合能力,可在短时间内改变生物体内的分子事件,同时还能通过化学修饰实现对特定细胞类型或亚细胞结构的靶向调控,为研究复杂生物系统提供了更具灵活性和精确性的技术策略,成为连接化学与生命科学的重要纽带。化学遗传技术的应用范围非常广,涵盖了神经科学、药物开发、信号转导和功能基因组学等多个领域。化学膜片钳技术原理
光遗传学技术的基本原理是利用光敏分子作为报告基因,将其导入到细胞或生物体内。化学膜片钳技术原理
光遗传膜片钳技术平台为神经科学研究带来了全新的视角与方法。在神经环路研究中,可通过光刺激特定神经元,利用膜片钳记录下游神经元的电反应,从而解析神经信号的传递路径与调控机制,帮助理解大脑信息处理的复杂过程。对于学习记忆等高级神经功能的研究,该平台能够精确操控参与记忆形成的神经元,记录其在记忆编码、存储和提取过程中的电活动变化,为揭示记忆的神经生物学基础提供关键数据,推动神经科学领域对大脑奥秘的深入探索。化学膜片钳技术原理
- 宁波光遗传膜片钳技术应用 2025-06-23
- 上海化学膜片钳技术原理 2025-06-23
- 合肥光遗传膜片钳技术服务 2025-06-23
- 漳州化学膜片钳技术方案 2025-06-23
- 嘉兴光遗传膜片钳技术 2025-06-23
- 蚌埠化学遗传技术服务公司 2025-06-23
- 绍兴光遗传膜片钳技术用途 2025-06-22
- 宁波原位杂交哪家好 2025-06-22
- 温州化学膜片钳技术哪家靠谱 2025-06-22
- 广州光遗传膜片钳技术服务中心 2025-06-22
- 山西奥索锐欧仿生磁腔大腿假肢 2025-06-23
- 先端子午流注 2025-06-23
- 上海菌燕益生元组合配方 2025-06-23
- 松江区医药ASAP技术稳定性预测 2025-06-23
- 妇科手术床采购 2025-06-23
- 佳木斯中医穴位针灸实训教学系统 2025-06-23
- 河南中风缺血预适应训练仪什么意思 2025-06-23
- 中医院艾灸仪24小时服务 2025-06-23
- 大肠肠道菌群检测方式 2025-06-23
- 合肥亲水涂层价格 2025-06-23