芜湖药理学膜片钳成像网站
膜片钳技术在通道研究中的重要作用:应用膜片钳技术可以直接观察和分辨单离子通道电流及其开闭时程、区分离子通道的离子选择性、同时可发现新的离子通道及亚型,并能在记录单细胞电流和全细胞电流的基础上进一步计算出细胞膜上的通道数和开放概率,还可以用以研究某些胞内或胞外物质对离子通道开闭及通道电流的影响等。同时用于研究细胞信号的跨膜转导和细胞分泌机制。结合分子克隆和定点突变技术,膜片钳技术可用于离子通道分子结构与生物学功能关系的研究。被孤立的小膜片面积为微米数量级,因此封接范围内细胞膜光有少数离子通道。芜湖药理学膜片钳成像网站
膜片钳的数据如何处理:全细胞式膜片方式使细胞内与浴槽之间的漏流极少。电极本身阻抗(1~10mω)与细胞封接后的阻抗相比较低,这种低接触阻抗使单管电压钳容易实现。电极管内与细胞之间弥散交换与平衡快,因而容易控制细胞内液的成分。细胞钳记录的是许多通道的平均电流,有利于综合分析。如果有目的地将膜电位钳制在某一程度,可做到选择性抑制某些通道的活性而只记录某种通道电流的总和,并可在同一细胞上观察几种不同通道的情况。通过改变内部介质,如改变电极液成分,或在电极液中加入所需药物,通过渗透很快改变胞浆成分并达到平衡,该手段在全细胞记录中广泛应用。芜湖药理学膜片钳成像网站膜片钳技术是在电压钳技术基础上发展起来的。
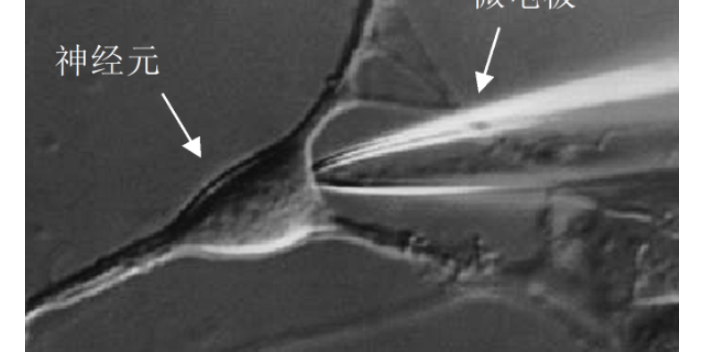
膜片钳技术与其他生物检测技术的结合应用:1.膜片钳与光学显微成像技术结合应用:利用激光扫描共聚焦显微镜、双光子显微镜、荧光显微镜等技术可以对细胞进行实时成像研究,将膜片钳技术与光学显微成像技术结合使用不但可以检测细胞的电流变化情况,而且还可以对细胞的电信号传递活动进行成像观察。2.膜片钳与原子力显微镜结合应用:将膜片钳和AFM结合使用的技术可以提高细胞电生理检测的分辨率和灵敏度;而且,在获得细胞电生理信息的同时,还能获取细胞的生物力学性质,从而更很全地研究细胞的生理功能。
膜片钳使用的注意事项:工作原理膜片钳是一种能够直接观察单一的离子通道蛋白质分子对相应离子通透难易程度等特性的一种实验技术。它的基本原理是以一个光洁,直径约为0.5~3um的玻璃微电极同神经或肌细胞的膜接触,之后对微电极另一端开口处施加适当的负压用电极的纤细开口将与电极接触的那一小片膜轻度吸入,如此在微电极开口处的玻璃边沿以及这一小片膜周边会形成紧密的封接,它的电阻能够达到数个或数十个千兆欧,这世界上就是在化学上完全隔离了吸附在微电极开口处的那一片膜同膜的其余部分,通过微电极记录到的电流变化光光和该膜片中通道分子的功能状态相关联。膜片钳技术用特制的玻璃微吸管吸附于细胞表面,使之形成10~100MΩ的高阻封接,被孤立的小膜片面积为微米数量级,因此封接范围内细胞膜光有少数离子通道。为了测量在不同药物对细胞中的离子通道的影响,通常需要在膜片钳实验中实施灌流。
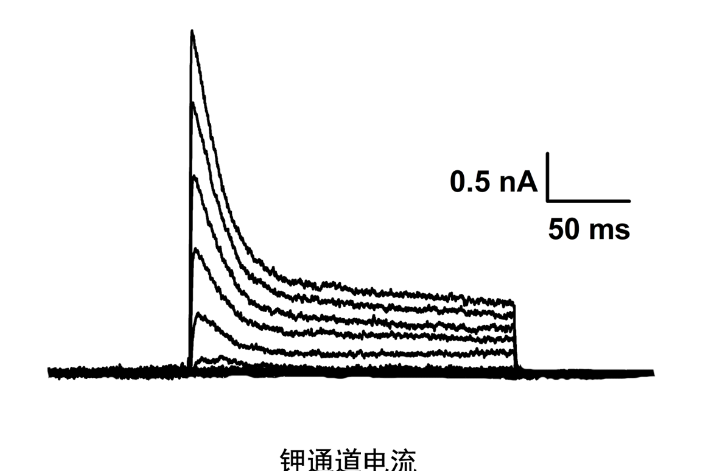
膜片钳记录的几种形式:细胞吸附膜片(cell-attached patch) 将两次拉制后经加热抛光的微管电极置于清洁的细胞膜表面上,形成高阻封接,在细胞膜表面隔离出一小片膜,既而通过微管电极对膜片进行电压钳制,高分辨测量膜电流,称为细胞贴附膜片。由于不破坏细胞的完整性,这种方式又称为细胞膜上的膜片记录。此时跨膜电位由玻管固定电位和细胞电位决定。因此,为测定膜片两侧的电位,需测定细胞膜电位并从该电位减去玻管电位。从膜片的通道活动看,这种形式的膜片是极稳定的,因细胞骨架及有关代谢过程是完整的,所受的干扰小。膜片钳使用操作流程及注意事项:在仪器使用以前及使用之后按按照使用时长做好登记工作。芜湖药理学膜片钳成像网站
膜片钳系统有如下应用局限性:在纪录对象上,目前的膜片钳系统只能纪录胞膜形状平整饱满的细胞。芜湖药理学膜片钳成像网站
膜片钳技术的基本原理和方法:膜片钳使用的基本方法是,把经过加热抛光的玻璃微电极在液压推进器的操纵下,与清洁处理过的细胞膜形成高阻抗封接,导致电极内膜片与电极外的膜在电学上和化学上隔离起来,由于电性能隔离与微电极的相对低电阻(1~5MΩ)只要对微电极施以电压就能对膜片进行钳制,从微电极引出的微小离子电流通过高分辨、低噪声、高保真的电流-电压转换放大器输送至电子计算机进行分析处理。膜片钳技术实现的关键是建立高阻抗封接,并能通过特定的记录仪器反映这些变化。芜湖药理学膜片钳成像网站
- 宁波光遗传膜片钳技术应用 2025-06-23
- 上海化学膜片钳技术原理 2025-06-23
- 合肥光遗传膜片钳技术服务 2025-06-23
- 漳州化学膜片钳技术方案 2025-06-23
- 嘉兴光遗传膜片钳技术 2025-06-23
- 绍兴光遗传膜片钳技术用途 2025-06-22
- 宁波原位杂交哪家好 2025-06-22
- 温州化学膜片钳技术哪家靠谱 2025-06-22
- 广州光遗传膜片钳技术服务中心 2025-06-22
- 淮南化学遗传技术原理 2025-06-22
- 妇科手术床采购 2025-06-23
- 佳木斯中医穴位针灸实训教学系统 2025-06-23
- 大肠肠道菌群检测方式 2025-06-23
- 甘肃假肢厂商 2025-06-23
- 华东补牙水门汀用法 2025-06-23
- 国产全自动核酸提取仪 2025-06-23
- 福建专业的病理实验外包推荐 2025-06-23
- 贵州卒中缺血预适应训练仪保健 2025-06-23
- 里昂矫形器要多少钱 2025-06-23
- 行走平衡测试系统器材 2025-06-23