诱导蛋白表达条件筛选
无细胞蛋白表达技术因其操作简单、周期短,已成为生物教学的理想工具。学生可在实验课中直接观察绿色荧光蛋白(GFP)的实时合成过程,直观理解中心法则。在科研中,CFPS被用于研究翻译调控机制、核糖体功能等基础问题,例如通过添加特定抑制剂分析蛋白质合成的能量依赖性。从药物开发到合成生命,无细胞蛋白表达技术的应用覆盖了生物医学、工业生物技术和基础研究。其hexin价值在于打破细胞壁垒,实现“按需合成”,未来随着自动化与微流控技术的结合,应用场景将进一步扩展。CHO细胞重组蛋白表达??是生产抗体的常用技术。诱导蛋白表达条件筛选

从实验室走向产业化,无细胞蛋白表达技术还面临多重障碍。规模化生产时,反应体系的均一性和重复性难以保证,且大规模制备高活性裂解物的成本效益比仍需优化。在下游纯化环节,由于反应混合物中含有大量核酸、酶和其他细胞组分,目标蛋白的分离纯化步骤比传统方法更复杂。此外,目前大多数CFPS工艺仍处于分批反应模式,连续化生产设备的开发滞后,限制了其在工业流水线中的应用潜力。尽管存在这些挑战,随着微流控技术、人工智能优化反应条件等新方法的引入,CFPS技术正在逐步突破这些产业化瓶颈。差异蛋白表达市场现状添加纳米盘磷脂的 ?GPCR体外蛋白表达??系统,功能性受体得率提升至80%。

国内生物医药行业对CFPS的价值认知不足,传统企业更依赖成熟的细胞表达系统(如CHO、大肠杆菌)。许多药企认为无细胞蛋白表达技术只适用于“科研级小试”,对其在药物开发(如ADC定点偶联)、mRNA疫苗抗原快速制备等工业化潜力持观望态度。同时,无细胞蛋白表达技术在复杂蛋白表达(如糖基化抗体)上的局限性也削弱了市场信心。相比之下,欧美已形成“CRO+药企”的协同生态(如Moderna与CFPS服务商合作),而国内缺乏此类模范案例,导致技术推广缺乏驱动力。
体外蛋白表达系统的本质是利用 纯化的细胞裂解物(含核糖体、tRNA、翻译因子及能量再生组分)重构蛋白质合成机器。在ATP/GTP供能条件下,核糖体通过mRNA模板介导的密码子-反密码子配对,驱动氨基酸按序列聚合成肽链。该过程的关键调控点包括:翻译起始效率(受5'UTR二级结构及Shine-Dalgarno序列影响)、延伸速率(依赖EF-Tu/G因子浓度)和终止准确性(释放因子RF1/2活性)。体外蛋白表达的高效性源于其 去除了细胞膜屏障,使反应底物浓度可人为提升至生理水平的10-100倍,大幅加速肽链合成动力学。使用T7 RNA聚合酶合成加帽mRNA,可提升??真核体外蛋白表达??效率。
在合成生物学中,无细胞蛋白表达技术是构建人工细胞和基因电路的he xin工具。研究人员通过混合不同物种(如大肠杆菌+哺乳动物)的裂解物,创建杂合翻译系统,以实现跨物种蛋白的协同合成。该技术还支持无细胞基因线路的快速原型设计,例如将CRISPR组分与报告蛋白共表达,用于体外诊断工具的开发。由于摆脱了细胞膜的限制,CFPS可直接整合非生物元件(如合成聚合物或纳米材料),推动人工合成生命和生物-非生物杂合系统的前沿研究。无细胞蛋白表达技术可快速表达膜蛋白(如GPCRs、离子通道)用于药物靶点研究,解决了此类蛋白在细胞内难表达、易沉淀的问题。在诊断领域,基于CFPS的体外转录-翻译系统被整合到便携式设备中,用于现场检测病原体核酸(如埃博拉病毒),实现“样本进-结果出”的快速诊断。此外,该技术还能合成定制化抗原,用于抗体库筛选或个性化cancer疫苗开发。用微流控技术整合裂解物分配\DNA模板加载及反应监测模块可在??单张芯片上并行执行千次蛋白表达反应??.常用蛋白表达行业动态
PCR纯化后的线性DNA模板可直接用于??大肠杆菌体外蛋白表达??。诱导蛋白表达条件筛选
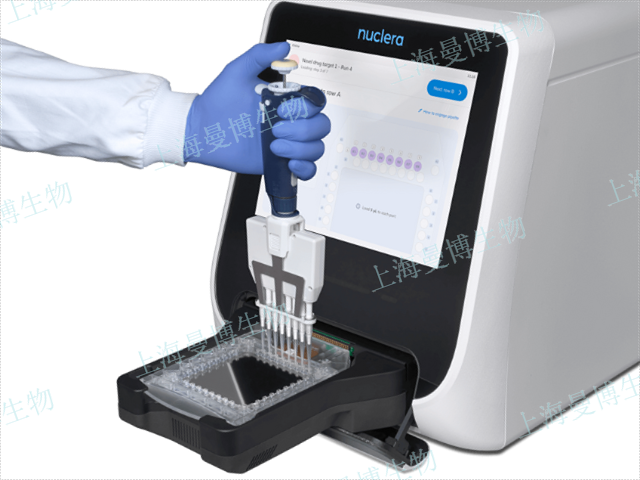
体外蛋白表达正在推动 无细胞合成生物学 的范式革新:人工代谢通路重构: 在裂解物中整合多酶级联反应,利用底物通道效应实现小分子化合物的高转化率合成;基因振荡器开发: 通过T7 RNA聚合酶的自调控表达构建分子钟,模拟细胞周期节律;仿生细胞构建: 将蛋白表达系统封装于脂质体内,结合ATP再生模块(如bing tong酸激酶系统)创建可自我维持的人工细胞雏形。这种 “设计-构建-测试”闭环 明显加速了生物系统的理性设计进程。nuclera 高通量微流控蛋白表达筛选系统可助力体外蛋白表达,如想了解更多信息,欢迎咨询官方代理商上海曼博生物!诱导蛋白表达条件筛选
- 肠道类器官芯片授权代理商 2025-07-31
- 高质量CRM197价格 2025-07-30
- 线性PEI转染试剂价格 2025-07-30
- GMP级慢病毒转导增强策略 2025-07-30
- 浙江MCECRM197 2025-07-30
- 原装CRM197回输人体 2025-07-30
- Thermo FisherPEI转染试剂价格多少 2025-07-30
- RNAPEI转染试剂病毒产量 2025-07-30
- RNAPEI转染试剂怎么样 2025-07-30
- 国产PEI转染试剂protocol 2025-07-30
- 四川医用助行器加盟 2025-07-31
- 苏州一次性医疗器械产品设计开发公司推荐 2025-07-31
- 上海特优级FBS技术指导 2025-07-31
- 山东3D医用刻录机功能强大 2025-07-31
- 衢州呼吸重症吊桥 2025-07-31
- 哪里有分析试剂共同合作 2025-07-31
- 贵州rb眼球保留义眼价格 2025-07-31
- 慈溪显微镜 2025-07-31
- 深圳名优生物试剂专卖店 2025-07-31
- 冠层光合速率多通道冠层光合仪多少钱一台 2025-07-31