芜湖原料药eCTD使用
美国药物主文件(Drug Master File, DMF)是向FDA提交的机密技术文件,用于支持药品生产、质量控制及合规性审查。以下为申报的要点和流程总结: DMF概述与类型 ?定义与作用 DMF是药品生产全过程的详细档案,包含原料药、辅料、包装材料等的生产设施、工艺、质量控制等信息,供制剂厂商引用以支持其注册申请。其意义在于保护企业机密的同时,满足FDA对供应链透明度的要求。 ?DMF类型 ?Ⅱ类:原料药、中间体及制剂(如微生物外泌体、细胞株等生物制品均属此类)。 ?Ⅲ类:包装材料。 ?Ⅳ类:辅料、着色剂等添加剂。 ?Ⅴ类:非临床/临床数据等特殊信息(需FDA预先批准)。 注:Ⅰ型(生产设施与人员)已于2000年停用。加拿大eCTD申报相关技术支持。芜湖原料药eCTD使用
欧盟eCTD的历史沿革与强制实施 欧盟自2003年逐步推进eCTD(电子通用技术文档)的标准化进程,初要求药注册申请(MAA)采用CTD格式。2010年,集中审评程序(CP)率先强制使用eCTD,随后分散程序(DCP)和互认程序(MRP)分别于2015年、2017年跟进。至2019年,欧盟要求所有国家程序(NP)的注册申请均以eCTD格式提交,标志着其电子递交体系的成熟。2024年,EMA启动eCTD4.0试点项目,旨在提升技术兼容性与审评效率。 eCTD验证标准的迭代与关键更 欧盟的验证标准历经多次调整,例如2025年3月启用的eCTD3.1区域模板和验证规则v8.1,对文件结构、元数据和内容完整性提出更严格的要求。标准引入的“追踪表(Tracking Table)”强制校验规则(如15.11和15.12)曾导致CEP(欧洲药典适用性证书)递交,后通过允许占位文件临时解决。与早期版本相比,v8.1强化了对模块一区域信息的逻辑验证,并细化了对PDF书签、超链接的规范性检查。太仓药品注册eCTD供应商欧盟NDA注册申报相关技术支持。
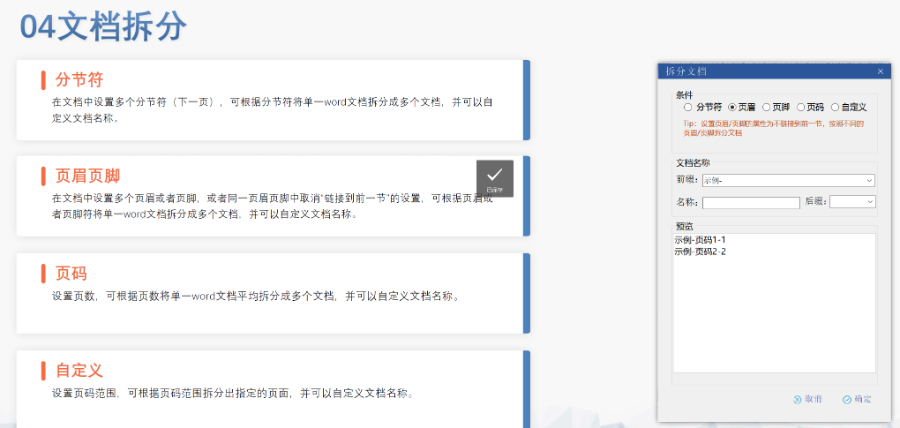
eCTD文件制作需遵循严格的法规要求和标准化流程,以下是关键要点整理:eCTD采用模块化结构,包含模块1(行政信息)至模块5(临床报告),需按ICH和监机构要求构建目录树。颗粒度选择:文件提交层级需在***申报时确定并沿用,例如原料和制剂的章节(如、)需按比较低颗粒度拆分,辅料单独成章。PDF需添加书签(导航目录)和超链接(跨网页跳转),超过5页的文件必须包含目录(TOC/LOT/LOF)。技术参数:初始视图需设置默认缩放级别和页面布局,书签展开层级不超过三级,单文件大小需符合申报系统限制。验证工具:使用软件(如BXeCTD)自动生成书签和超链接,并通过序列校验和PDF校验功能确保合规性。
eCTD 4.0版本的过渡与升级:FDA于2023年启动eCTD 4.0技术试点,2024年9月正式接收申请,计划2029年完成全过渡。4.0版本改用HL7 RPS标准替代XML,支持双向通信和跨申请文件复用,例如同一Study ID可在IND和NDA享。模块1的校验码从MD5升级为SHA-256,主干文件由改为,序列号取消前导零(如“1”而非“0001”)。企业需同步更软件系统以适应架构。DMF与IND申报的特殊要求:针对Type II(原料药)和Type IV(辅料)DMF,eCTD模块3需详细描述生产工艺、稳定性数据,并附分析证书(COA)。FDA要求DMF持有人指定美国境内代理人,确保沟通效率,且LOA(授权书)需明确引用范围。IND安全性报告(如SUSAR)需通过eCTD模块5.3.5提交,15天内完成,并嵌入CIOMS或MedWatch表格。2024年指南强调,临床数据库需以SAS XPORT格式提交,单个文件超过4GB需拆分并说明规则。中NDA注册申报相关技术支持。

电子签章与传输安全 文件需经AES-256加密后刻录至不可擦写光盘,并附MD5校验码。光盘损坏或病毒污染将触发重递交流程,原载体按销毁程序处理。 ?审评与核查协同 自2018年起,FDA要求提交两套光盘分别用于审评和现场核查,2022年调整为“1套审评+1套核查+1套专项资料”模式,提升流程效率。 ?国际化兼容性增强 美国eCTD系统支持与欧盟、日本等地区的XML互操作性,但区域差异(如模块1的标签要求)仍需人工适配。 ?未来通道创 FDA计划引入API接口支持企业系统直连,并探索基于云存储的实时提交与审评,减少物理媒介依赖。欧盟eCTD验证标准相关技术支持。太仓药品注册eCTD供应商
欧盟CESP提交通道相关技术支持。芜湖原料药eCTD使用
美国eCTD的强制实施时间与范围:美国自2017年5月5日起要求药申请(NDA)、仿制药申请(ANDA)和生物制品许可申请(BLA)必须通过eCTD格式提交,2018年5月5日进一步扩展至临床试验申请(IND)和药品主文件(DMF)。FDA通过《联邦食品、药品和化妆品法案》第745A条明确电子提交的强制性,豁免非商业化IND和部分DMF类型(如Ⅲ类)。2023年数据显示,FDA接收的eCTD申请占比已达92%,标志着电子化审评体系的成熟。企业若未按规范提交(如缺少文件或重复序列号),将直接被拒收。芜湖原料药eCTD使用
- 高新区中国eCTD欢迎选购 2025-05-14
- 静安区生物制品eCTD使用 2025-05-14
- 芜湖新药eCTD是什么 2025-05-14
- 吴江区赋悦科技eCTD供应商 2025-05-14
- 南京生物制品eCTD注册系统 2025-05-14
- 上海化学药品eCTD格式 2025-05-09
- 南京电子申报eCTD哪个品牌好 2025-05-09
- 太仓NDAeCTD服务价格 2025-05-09
- 浦东新区原料药eCTD文件如何制作 2025-04-26
- 南京新药eCTD找哪家 2025-04-26
- 鼓楼区现代数据定向分析 2025-06-07
- 湖南巡检养老机器人定制 2025-06-07
- 杭州消费电子类线束 2025-06-07
- 家校互联视频话机厂家批发 2025-06-07
- 淮安特殊光解膜厂家直销 2025-06-07
- 自动化曝光引流价格行情 2025-06-07
- 湖北正版ANSYS HFSS 2025-06-07
- 吉林工业一体机生产厂家 2025-06-07
- 重型智能营销产品 2025-06-07
- 浙江RFID通道门销售公司 2025-06-07