浙江国内注册eCTD常用解决方案
从纸质到电子的历史过渡 2017年前,美国允许纸质与eCTD并行提交,但此后逐步淘汰纸质通道,保留紧急情况下的例外审批。2020年电子化后,所有IND、NDA、ANDA和DMF强制采用eCTD格式。 ?系统平台升级 FDA通过“药品业务应用系统”和“药品eCTD注册系统”实现电子资料接收、受理与审评的全流程数字化。2022年系统增自动推送受理文书和短信提醒功能,减少人工干预。 ?电子文档结构优化 美国eCTD采用分层文件夹结构,例如化学药品的模块1-5分别对应行政文件、总结报告、质量数据等。2020年后增“临床试验数据库”装盒要求,强化数据可追溯性。澳大利亚eCTD申报软件相关技术支持。浙江国内注册eCTD常用解决方案

紧急申报与特殊通道:FDA设置紧急申报通道(如Pre-EUA和EUA),允许在公共卫生事件中快速提交资料。此类申请需在模块1.19注明特殊标识,并通过ESG加急处理。 eCTD版本兼容性与过渡策略:eCTD 4.0支持向前兼容,允许v3.2.2文件无缝过渡。企业需在2024年前完成系统升级,确保XML到HL7 RPS的格式转换。过渡期间需同时维护旧版本系统。 区域差异与全球化协调:美国模块1要求严格,如UUID标识符和组合申请支持,而欧盟侧重文件引用合规性。FDA与PMDA、EMA通过ICH框架协调eCTD标准,但区域特殊性仍需针对性适配。 行业影响与长期价值:eCTD不是技术升级,更是全球药品监管一体化的驱动力。其标准化、可追溯性和效率提升,推动了跨国多中心试验的协同申报,加速创药上市进程。云南国内注册eCTD美国IND注册申报相关技术支持。
DMF维护与合规 ?年度更 即使无变更,每年需提交声明;重大工艺/设施变更需及时通知客户并更文件。 ?现场检查 原料药企业需通过FDA现场检查,验证是否符合ICH Q7 GMP标准,并与DMF内容一致。 ?转让与关闭 ?转让:需书面通知FDA并提供持有者信息。 ?关闭:未提交年度报告或持有人主动申请,需说明原因并通知所有授权方。 关键注意事项 ?数据质量:所有资料需准确、完整,减少审核延迟风险。 ?合规性:遵循FDA指南(如21 CFR Part 207)及USP标准(如培养基物料来源级别)。 ?沟通机制:建议通过专业机构(如瑞欧佰药)协助,定期提交周报并制定计划表以提高效率。 常见问题解答 ?生物制品分类:培养基、外泌体等均属Ⅱ类DMF。 ?质量标准:参考USP及同行标准,需提供分析方法验证及杂质对比研究。 ?周期估算:资料准备约5-50个工作日,总周期受缺陷回复影响。
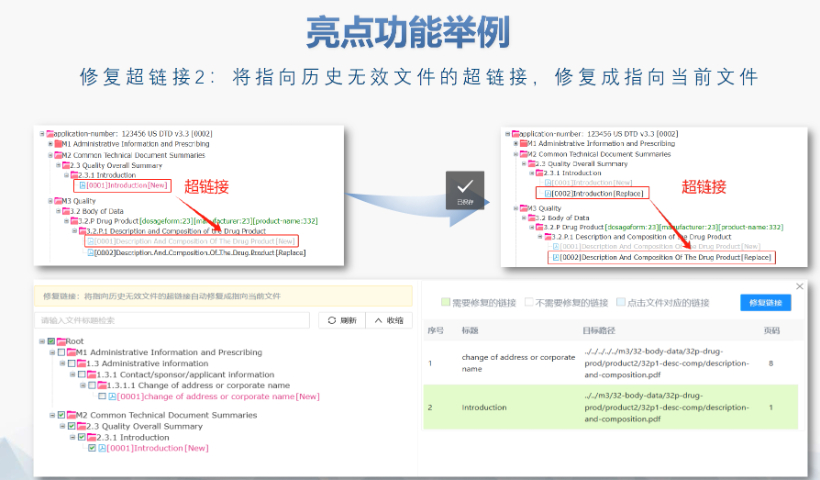
文件生命周期管理:eCTD支持文件替换(Replace)、删除(Delete)等操作,而非增文件。例如,更临床研究方案时需用Replace操作覆盖旧版本。基线提交(Baseline Submission)可用于补充历史纸质资料,但需在封面函中声明无内容变更。 临床数据与研究标签文件(STF):模块4和5中的研究数据需通过STF(Study Tagging Files)引用,确保数据与文档关联。FDA要求数据集(如SAS XPORT格式)能置于模块3-5,且单个文件超过4GB需拆分。2022年统计显示,58%的ANDA因研究数据技术拒绝标准(TRC)错误被拒。 电子签名与表格要求:FDA表格(如356h、1571)需使用数字签名,PDF文件禁止加密或设置编辑限制。电子签名需符合21 CFR Part 11规范,确保身份验证、不可否认性和数据完整性。 外包服务与系统解决方案:赋悦科技累计提交超2000份eCTD申请,外包可降低40%人工错误率。瑞士eCTD验证标准相关技术支持。
电子签章与安全性 FDA要求所有PDF文件需经数字签名,并通过MD5校验确保传输完整性。签章需符合21 CFR Part 11的电子记录规范,部分情况下允许临时放宽(如期间的远程签署)。 ?多模块协同验证 模块1(行政文件)的区域性元数据(如申请类型、联系人信息)需与模块2-5的内容逻辑一致。例如,生物制品的3.2.R扩展节点命名需遵循特定规则,而化学药品则禁止使用此类扩展。 ?验证工具与流程 主流工具如LORENZ eValidator支持自动化验证,生成包含错误定位与修复建议的详细报告。企业需在提交前完成内部验证,并通过“药品业务应用系统”推送受理状态。 ?常见问题与规避策略 高频错误包括PDF安全设置、书签链接失效、STF(研究标签文件)缺失等。例如,未在5.3.1章节标注研究ID会导致验证警告,需通过说明函解释。企业可通过建立标准化模板库和预检流程降低风险。 ?后续监管与更 FDA定期更验证标准(如2022年增临床试验数据完整性检查),企业需通过订阅官方通知或第三方服务商获取动态欧盟DMF注册申报相关技术支持。宁波国内注册eCTD常用解决方案
加拿大IND注册申报相关技术支持。浙江国内注册eCTD常用解决方案
审评效率与时间线优化 eCTD的标准化缩短了审评周期:集中程序平均审评时间从18个月降至12个月,互认程序可在90天内完成成员国意见协调。自动化验证工具减少了格式错误导致的退审率,但复杂药学数据的科学审评仍需较长时间。申请人可通过预提交会议(Pre-submission meeting)提前沟通技术细节,规避潜在延误。 区域协作与全球互认 欧盟通过互认程序与澳大利亚、加拿大等国实现eCTD数据共享,CEP证书在40余个非欧盟国家有效。然而,模块一区域信息的差异性仍要求申请人定制化调整,例如亚洲国家可能要求附加稳定性研究数据。ICH的协调作用有助于减少重复提交,但完全全球化仍需解决法规和技术壁垒。 技术工具与行业生态 主流eCTD编辑软件(如Lorenz、Extedo)支持欧盟区域模板的自动化生成,并与验证工具集成实现一键校验。云平台解决方案逐渐普及,支持多国团队协同编辑和实时版本控制。然而,软件采购和维护成本较高,中小企业常选择外包给专业服务商完成递交。浙江国内注册eCTD常用解决方案
赋悦科技(杭州)有限责任公司是一家有着先进的发展理念,先进的管理经验,在发展过程中不断完善自己,要求自己,不断创新,时刻准备着迎接更多挑战的活力公司,在浙江省等地区的数码、电脑中汇聚了大量的人脉以及**,在业界也收获了很多良好的评价,这些都源自于自身的努力和大家共同进步的结果,这些评价对我们而言是比较好的前进动力,也促使我们在以后的道路上保持奋发图强、一往无前的进取创新精神,努力把公司发展战略推向一个新高度,在全体员工共同努力之下,全力拼搏将共同赋悦科技供应和您一起携手走向更好的未来,创造更有价值的产品,我们将以更好的状态,更认真的态度,更饱满的精力去创造,去拼搏,去努力,让我们一起更好更快的成长!
- 高新区中国eCTD欢迎选购 2025-05-14
- 静安区生物制品eCTD使用 2025-05-14
- 芜湖新药eCTD是什么 2025-05-14
- 吴江区赋悦科技eCTD供应商 2025-05-14
- 南京生物制品eCTD注册系统 2025-05-14
- 上海化学药品eCTD格式 2025-05-09
- 南京电子申报eCTD哪个品牌好 2025-05-09
- 太仓NDAeCTD服务价格 2025-05-09
- 浦东新区原料药eCTD文件如何制作 2025-04-26
- 南京新药eCTD找哪家 2025-04-26
- 定制SaaS智能营销云平台怎么用 2025-06-04
- 白山自媒体营销推广特点 2025-06-04
- 福建家用工控机箱品牌 2025-06-04
- 机械关于互联网软件加盟报价 2025-06-04
- 惠山区多功能共享云桌面价格 2025-06-04
- 河北企业源代码加密费用 2025-06-04
- 北京应用KISSsoft参数 2025-06-04
- 宁波储能线束定制 2025-06-04
- 安徽海外商城开发 2025-06-04
- 海口文书录像带数据转换 2025-06-04