吴江区CDE eCTD服务放心可靠
eCTD的实施为监管机构和企业带来了多重机遇。电子化申报资料能够极大地加速审评效率,减少人为判断错误和数据混淆的情况,从而提高审评的准确性和速度。同时,eCTD带来的数据标准化机遇使得全球监管机构的资料内容和电子格式得以统一,有助于在不同监管机构之间进行数据传输和共享。这对于提升全球监管效率和行业研发效率具有重要意义。 此外,eCTD的实施还促进了国际合作,构建了全球监管的底层大数据基础。对于企业而言,eCTD提供了一个规范化的研发活动模板,有助于降低与监管机构沟通的成本,提高申报效率。特别是对于国内的生物技术企业而言,eCTD的实施更是具有重要意义,有助于这些企业更好地走向国际市场。然而,中小企业在享受这些机遇的同时,也面临着技术和成本压力。eCTD的实施需要专门的团队进行系统维护和开发,这对于中小企业来说是一笔不小的开支。同时,数据安全问题也是企业关注的焦点。 此次CDE扩大eCTD实施范围对行业而言是一个积极的风向标。短期内,企业面临的挑战包括适应更高要求的技术规范并提高文件质量、和eCTD出版系统的磨合以及进行eCTD知识的跨职能培训等。 澳大利亚eCTD注册咨询相关技术支持。吴江区CDE eCTD服务放心可靠

美国于2003年成为全球早采用eCTD(电子通用技术文档)的国家之一,初由CDER和CBER作为电子提交平台试点。2008年起,eCTD正式成为药申请(NDA)和生物制品许可申请(BLA)的标准格式,并在2012年通过《药申报者付费法案》(PDUFA)进一步强化其法律地位。至2017年,FDA强制要求所有药申请(NDA)、简略药申请(ANDA)及药物主文件(DMF)必须采用eCTD格式提交,标志着其从可选到强制的转型。这一进程在2018年扩展至临床试验申请(IND),终实现全类型药品注册的电子化覆盖江苏仿制药eCTD医疗科技eCTD申报软件相关技术支持。
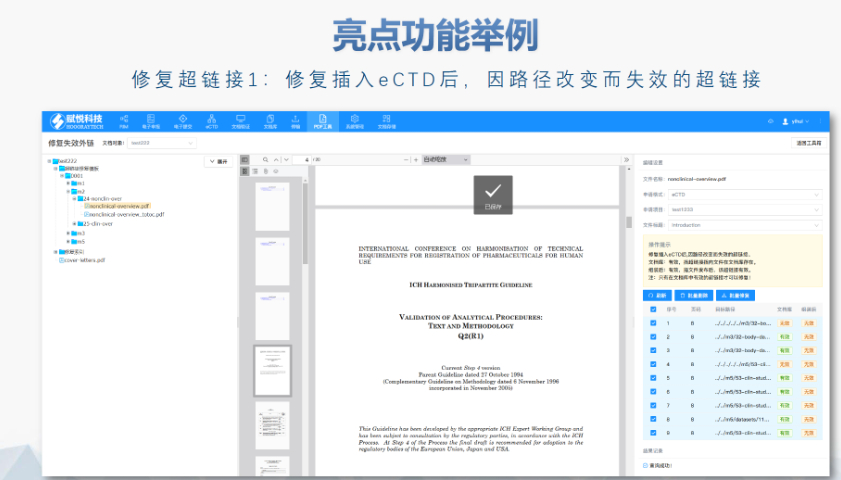
DMF维护与合规 ?年度更 即使无变更,每年需提交声明;重大工艺/设施变更需及时通知客户并更文件。 ?现场检查 原料药企业需通过FDA现场检查,验证是否符合ICH Q7 GMP标准,并与DMF内容一致。 ?转让与关闭 ?转让:需书面通知FDA并提供持有者信息。 ?关闭:未提交年度报告或持有人主动申请,需说明原因并通知所有授权方。 关键注意事项 ?数据质量:所有资料需准确、完整,减少审核延迟风险。 ?合规性:遵循FDA指南(如21 CFR Part 207)及USP标准(如培养基物料来源级别)。 ?沟通机制:建议通过专业机构(如瑞欧佰药)协助,定期提交周报并制定计划表以提高效率。 常见问题解答 ?生物制品分类:培养基、外泌体等均属Ⅱ类DMF。 ?质量标准:参考USP及同行标准,需提供分析方法验证及杂质对比研究。 ?周期估算:资料准备约5-50个工作日,总周期受缺陷回复影响。
美国药物主文件(Drug Master File, DMF)是向FDA提交的机密技术文件,用于支持药品生产、质量控制及合规性审查。以下为申报的要点和流程总结: DMF概述与类型 ?定义与作用 DMF是药品生产全过程的详细档案,包含原料药、辅料、包装材料等的生产设施、工艺、质量控制等信息,供制剂厂商引用以支持其注册申请。其意义在于保护企业机密的同时,满足FDA对供应链透明度的要求。 ?DMF类型 ?Ⅱ类:原料药、中间体及制剂(如微生物外泌体、细胞株等生物制品均属此类)。 ?Ⅲ类:包装材料。 ?Ⅳ类:辅料、着色剂等添加剂。 ?Ⅴ类:非临床/临床数据等特殊信息(需FDA预先批准)。 注:Ⅰ型(生产设施与人员)已于2000年停用。欧盟eCTD注册外包相关技术支持。
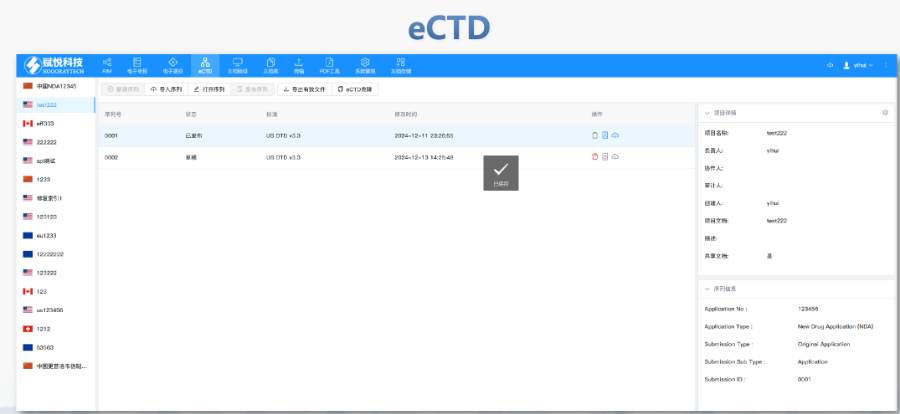
eCTD在欧盟药品监管中的历史背景:欧盟eCTD(电子通用技术文档)的发展始于对临床试验和药品审评流程标准化的需求。2001年,欧盟引入《临床试验指令》(CTD)作为统一的法律框架,但其分散的成员国申报机制导致效率低下。2014年,欧盟通过《临床试验法规》(CTR, Regulation EU No. 536/2014),要求通过CTIS平台(临床试验信息系统)集中提交临床试验申请(CTA),并逐步推动eCTD作为电子化申报的工具。这一旨在解决传统CTD模式下审评周期长、多国协调成本高的问题,为eCTD的实施奠定了基础。瑞士IND注册申报相关技术支持。徐汇区赋悦科技eCTD名称
澳大利亚DMF注册申报相关技术支持。吴江区CDE eCTD服务放心可靠
欧盟eCTD的递交途径与技术要求 不同审评程序对应不同递交渠道:集中程序(CP)通过EMA的eSubmission Gateway或Web Client提交,分散程序(DCP)和互认程序(MRP)则需使用欧盟通用提交门户(CESP)。文件结构需严格遵循模块化要求,例如CEP申请需包含模块1(行政文件)、模块2(质量概述)和模块3(技术文档),且XML主干文件须符合EDQM的特定命名规则。此外,所有PDF文件需无密码保护、可全文检索,并嵌入层级书签以支持快速审阅。 CEP申请的eCTD递交特殊性 CEP程序自2018年起强制采用eCTD格式,重点评估原料药是否符合欧洲药典标准。其模块1需包含EDQM申请表、简历及变更说明表,模块2需使用EDQM提供的质量概述模板,模块3则按CTD格式组织3.2.S章节内容。CEP与ASMF(活性物质主文件)的主要区别在于性:CEP无需关联上市许可,且审评由EDQM完成。吴江区CDE eCTD服务放心可靠
赋悦科技(杭州)有限责任公司汇集了大量的优秀人才,集企业奇思,创经济奇迹,一群有梦想有朝气的团队不断在前进的道路上开创新天地,绘画新蓝图,在浙江省等地区的数码、电脑中始终保持良好的信誉,信奉着“争取每一个客户不容易,失去每一个用户很简单”的理念,市场是企业的方向,质量是企业的生命,在公司有效方针的领导下,全体上下,团结一致,共同进退,**协力把各方面工作做得更好,努力开创工作的新局面,公司的新高度,未来赋悦科技供应和您一起奔向更美好的未来,即使现在有一点小小的成绩,也不足以骄傲,过去的种种都已成为昨日我们只有总结经验,才能继续上路,让我们一起点燃新的希望,放飞新的梦想!
- 高新区中国eCTD欢迎选购 2025-05-14
- 静安区生物制品eCTD使用 2025-05-14
- 芜湖新药eCTD是什么 2025-05-14
- 吴江区赋悦科技eCTD供应商 2025-05-14
- 南京生物制品eCTD注册系统 2025-05-14
- 上海化学药品eCTD格式 2025-05-09
- 南京电子申报eCTD哪个品牌好 2025-05-09
- 太仓NDAeCTD服务价格 2025-05-09
- 浦东新区原料药eCTD文件如何制作 2025-04-26
- 南京新药eCTD找哪家 2025-04-26
- 定制SaaS智能营销云平台怎么用 2025-06-04
- 白山自媒体营销推广特点 2025-06-04
- 福建家用工控机箱品牌 2025-06-04
- 机械关于互联网软件加盟报价 2025-06-04
- 惠山区多功能共享云桌面价格 2025-06-04
- 河北企业源代码加密费用 2025-06-04
- 北京应用KISSsoft参数 2025-06-04
- 宁波储能线束定制 2025-06-04
- 安徽海外商城开发 2025-06-04
- 海口文书录像带数据转换 2025-06-04