上海辅助生殖纺锤体液晶偏光补偿器
无需染色纺锤体观察技术能够实时监测冷冻过程中纺锤体的形态变化,从而准确评估冷冻保存的效果。通过对比冷冻前后纺锤体的形态和稳定性,研究者可以优化冷冻保护剂的配方和浓度,以及改进冷冻程序,减少冷冻损伤,提高解冻后卵母细胞的存活率和发育潜能。解冻后的卵母细胞在无需染色的情况下,可以直接通过Polscope系统进行纺锤体观察。这一技术能够迅速评估解冻后卵母细胞的质量,包括纺锤体的形态、位置、稳定性等关键指标,为后续的受精和胚胎发育提供重要参考。纺锤体的微管在细胞分裂后期会断裂并重新组装,形成新的细胞结构。上海辅助生殖纺锤体液晶偏光补偿器
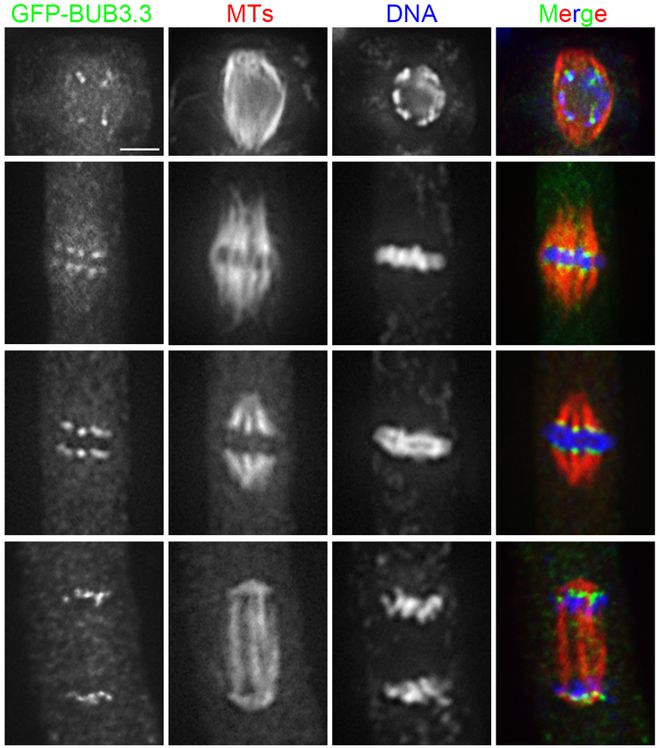
玻璃化冷冻技术因其快速冷冻和解冻的特点,在哺乳动物纺锤体卵冷冻保存中展现出巨大优势。该技术通过极快的降温速率和高浓度的冷冻保护剂,使细胞内溶液在冷冻过程中呈玻璃态而非结晶态,从而避免了冰晶对纺锤体的损伤。此外,研究者们还尝试将微流控技术、激光辅助冷冻等新技术应用于卵母细胞的冷冻保存中,以进一步提高冷冻效果。为了准确评估冷冻对纺锤体的影响,研究者们开发了多种纺锤体稳定性评估技术。例如,通过偏光显微镜观察纺锤体的形态变化;利用免疫荧光染色技术检测纺锤体相关蛋白的分布和表达;以及通过分子生物学方法检测纺锤体相关基因的转录和翻译水平等。这些技术的应用为深入研究冷冻过程中纺锤体的变化提供了有力支持。武汉双折射性纺锤体观测仪纺锤体在细胞分裂后期通过微管切割机制实现染色体分离。
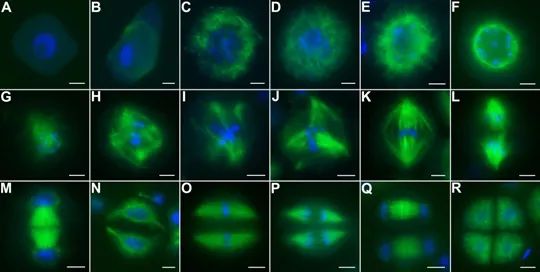
纺锤体在有丝分裂中发挥着至关重要的导航作用,其主要功能包括:排列与分裂染色体:纺锤体的完整性决定了染色体分裂的正确性。在细胞分裂中期,染色体在纺锤丝的牵引下,自动在赤道板排列整齐。当细胞进入分裂后期,纺锤体微管收缩,将染色体牵引至两极,形成两组数目相等的姐妹染色单体。这一过程确保了遗传信息的准确传递,避免了染色体分离错误导致的遗传异常。决定胞质分裂的分裂面:在染色体分裂的同时,纺锤体中的一部分微管不随染色体分裂到两极,而是停弛在纺锤体中间形成纺锤中心体。纺锤中心体的中心区域为两组极性相反的微管交叠区,称为纺锤中心区,它决定了接下来的胞质分裂面。胞质分裂开始于分裂后期的较晚期,一般结束于分裂末期后1-2小时,此期间两个子细胞由中心颗粒体连接。纺锤体通过精确控制胞质分裂面的位置,确保了细胞分裂的对称性和稳定性。
在有丝分裂中,纺锤体的形成与功能至关重要。首先,在有丝分裂前期,中心体复制并分离至细胞两极,形成纺锤体的两极。随后,微管从两极向中心区域延伸,形成纺锤体的主干。在中期,染色体在纺锤丝的牵引下,自动在赤道板排列整齐。当细胞进入分裂后期,纺锤体微管收缩,将染色体牵引至两极,形成两组数目相等的姐妹染色单体。这一过程确保了遗传信息的准确传递,避免了染色体分离错误导致的遗传异常。此外,纺锤体还决定了胞质分裂的分裂面。在染色体分裂的同时,纺锤体中的一部分微管不随染色体分裂到两极,而是停弛在纺锤体中心,形成纺锤中心体。纺锤中心体的中心区域为两组极性相反的微管交叠区,称为纺锤中心区,它决定了接下来的胞质分裂面。胞质分裂开始于分裂后期的较晚期,一般结束于分裂末期后1-2小时,此期间两个子细胞由中心颗粒体连接。纺锤体通过精确控制胞质分裂面的位置,确保了细胞分裂的对称性和稳定性。纺锤体微管与染色体上的动粒结合,形成稳定的连接。
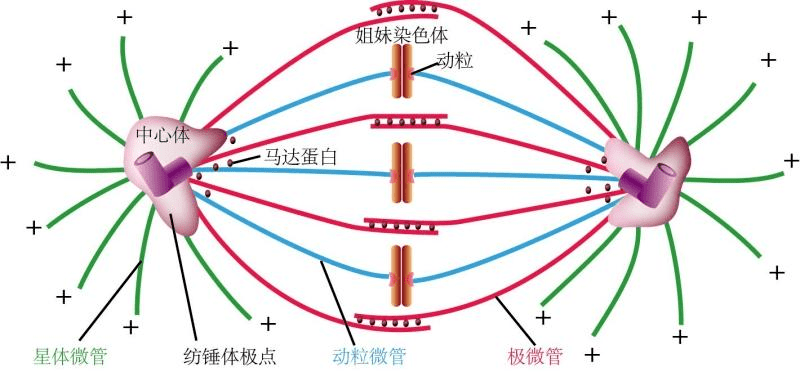
光学相干断层成像是一种基于低相干光干涉原理的成像技术,具有高分辨率、非侵入性和实时成像等特点。在纺锤体卵冷冻研究中,OCT技术可用于观察卵母细胞内部结构的细微变化,包括纺锤体的形态和位置。虽然目前OCT技术在纺锤体成像方面的应用还较为有限,但随着技术的不断发展和完善,相信未来OCT将在纺锤体卵冷冻研究中发挥更加重要的作用。虽然MRI和超声波成像在生殖医学中主要用于软组织的成像,如子宫、卵巢等病变检测,但它们在纺锤体卵冷冻研究中的应用也值得探讨。随着技术的不断进步,高分辨率MRI和超声波成像技术可能会实现对卵母细胞内部结构的更精细观察。研究纺锤体有助于理解细胞分裂的分子机制。上海ICSI纺锤体玻璃底培养皿
纺锤体的研究对于理解遗传信息的传递和维持具有重要意义。上海辅助生殖纺锤体液晶偏光补偿器
无需染色纺锤体观察技术已逐步应用于临床辅助生殖技术中。通过该技术,医生可以在不破坏卵母细胞活性的情况下,评估其质量并选择合适的卵母细胞进行受精和胚胎移植,从而提高妊娠率和胚胎质量。无需对卵母细胞进行固定和染色处理,保留了细胞的活性与完整性。能够实时监测冷冻过程中纺锤体的形态变化,评估冷冻效果。能够实时监测冷冻过程中纺锤体的形态变化,评估冷冻效果。Polscope偏振光显微成像系统的操作和维护需要较高的专业知识和技能。纺锤体的形态变化复杂多样,需要丰富的经验和专业知识进行数据解读和结果分析。上海辅助生殖纺锤体液晶偏光补偿器
- 美国人精子分析频闪光源 2025-06-06
- 北京前向运动精子分析VAP 2025-06-06
- 北京绵羊精子分析DAP 2025-06-06
- 广州水生动物精子分析ALH 2025-06-06
- 香港牛精子分析VCL 2025-06-06
- 美国PH实时监控时差培养箱胚胎评分 2025-06-06
- 北京浓度精子分析W.H.O 4 2025-06-06
- 北京精子分析DSL 2025-06-06
- 上海濒危物种精子分析 2025-06-06
- 深圳非侵入式成像纺锤体胚胎发育 2025-06-06
- 四川氧气检测仪生产厂家 2025-06-06
- 国外布鲁克双光子显微镜磷光寿命计数 2025-06-06
- 江西循环水压力变送器产品介绍 2025-06-06
- 温州美标弯头咨询 2025-06-06
- 苏州固定滑槽倾角计厂家直销 2025-06-06
- 光谱仪厂家电话 2025-06-06
- 贵州通风自力式询问报价 2025-06-06
- 黔西南在线安全阀校检机构 2025-06-06
- 北京稳定性高纤维直径检测设备哪里有 2025-06-06
- 湖北小型激光测距传感器 2025-06-06