昆明克隆纺锤体透明带
纺锤体观测仪在补救ICSI中的应用我们知道,成熟的卵母细胞含有1个极体,也就是***极体。IVF加入精子后,精子会穿透层层障碍**终进入卵子,随着时间的推移,~6小时后卵子的纺锤体会将染色单体拉向两极,进而排出第二极体,再往后大约加精后9~16小时,雌雄原核会出现,而原核的出现才是受精的标志。但是对于那些没有受精的卵子,到了原核出现的时间窗发现没有受精时再去补救ICSI,往往错过了卵子的比较好受精时间,因为没有受精的卵子会在体外老化,即使受精,胚胎的发育潜能也很低。所以,我们在加精后的4~6小时,通过观察第二极体的排出来初步判断是否受精,**的增加了那些受精障碍患者的受精率,也避免了卵子的老化。当然,偶尔也会出现错误补救。文献报道对IVF受精后的未排出第二极体的卵母细胞进行补救,实验组用纺锤体观测仪观察并统计纺锤体的数目,82.7%含有一个纺锤体,17.3%含有两个纺锤体,并对含有一个纺锤体的卵母细胞进行补救ICSI;而对照组并未用纺锤体观测仪观察纺锤体,只对未排出第二极体的卵母细胞进行补救ICSI。结果发现使用纺锤体观测仪观察纺锤体的数目能显著提高正常受精率,降低多原核受精比率。纺锤体由微管组成,其动态变化调控着细胞分裂的进程。昆明克隆纺锤体透明带
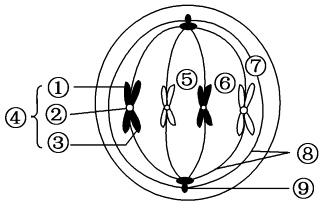
纺锤体是卵母细胞在减数分裂过程中形成的一种微管结构,负责精确分离染色体。然而,纺锤体对环境温度、渗透压等外部条件极为敏感,在冷冻保存过程中容易发生损伤,导致染色体分离异常,进而影响卵母细胞的发育潜力和受精后的胚胎质量。因此,如何有效监测和评估冷冻过程中纺锤体的变化,成为纺锤体卵冷冻研究的重要课题。纺锤体实时成像技术的出现,为这一问题的解决提供了可能。纺锤体实时成像技术主要利用高分辨率显微镜结合荧光标记技术,对卵母细胞内的纺锤体进行实时、动态的观察和记录。常用的荧光标记方法包括使用绿色荧光蛋白(GFP)标记微管蛋白,以及利用特定抗体对纺锤体相关蛋白进行染色。通过这些方法,研究者可以清晰地观察到纺锤体的形态、位置、动态变化等信息,从而准确评估冷冻过程中纺锤体的稳定性和完整性。北京偏光成像纺锤体兼容大部分显微镜纺锤体的形成需要多种蛋白质的精确协作与调控。
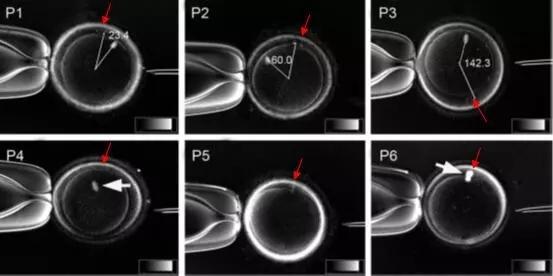
在纺锤体卵冷冻过程中,利用纺锤体实时成像技术可以实时监测纺锤体的变化。通过观察冷冻过程中纺锤体的形态、位置及动态变化,研究者可以判断冷冻保护剂的效果、冷冻速率等因素对纺锤体的影响,从而优化冷冻方案,减少纺锤体损伤。解冻后,利用纺锤体实时成像技术可以对卵母细胞内的纺锤体进行再次评估。通过比较解冻前后纺锤体的形态和稳定性,研究者可以判断冷冻过程对纺锤体的损伤程度,并筛选出纺锤体形态完好的卵母细胞进行后续操作,提高受精率和胚胎发育质量。
光学相干断层成像是一种基于低相干光干涉原理的成像技术,具有高分辨率、非侵入性和实时成像等特点。在纺锤体卵冷冻研究中,OCT技术可用于观察卵母细胞内部结构的细微变化,包括纺锤体的形态和位置。虽然目前OCT技术在纺锤体成像方面的应用还较为有限,但随着技术的不断发展和完善,相信未来OCT将在纺锤体卵冷冻研究中发挥更加重要的作用。虽然MRI和超声波成像在生殖医学中主要用于软组织的成像,如子宫、卵巢等病变检测,但它们在纺锤体卵冷冻研究中的应用也值得探讨。随着技术的不断进步,高分辨率MRI和超声波成像技术可能会实现对卵母细胞内部结构的更精细观察。纺锤体的一端连接着染色体,另一端则锚定在细胞两极。
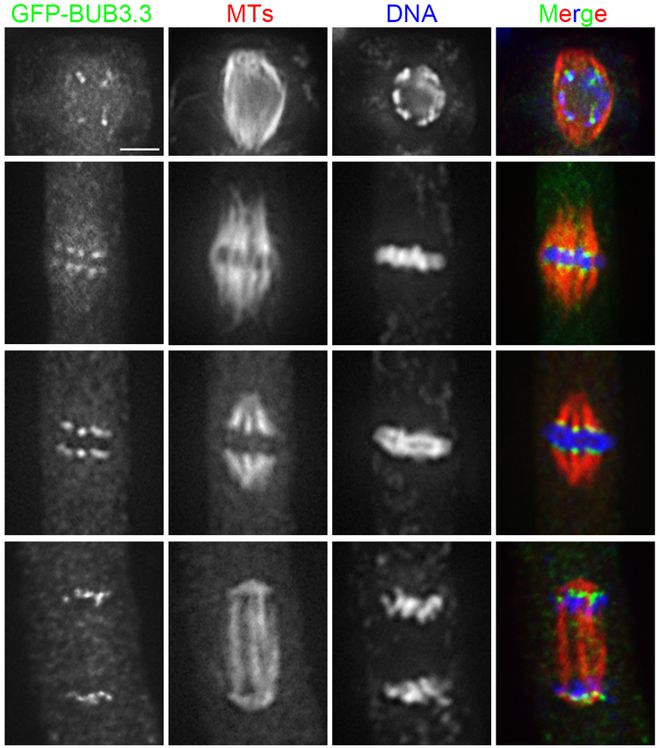
随着科技的不断发展,无损观察技术将不断得到优化和创新。未来有望开发出更加便捷、高效、低成本的成像设备,进一步降低设备成本并提高操作简便性。同时,通过优化成像算法和数据处理技术,可以实现对纺锤体形态变化的更精细、更准确的评估。无损观察纺锤体卵冷冻研究涉及生殖医学、细胞生物学、材料科学等多个领域。未来通过加强不同学科之间的交叉融合和协同创新,可以推动该领域取得更多突破性进展。例如,结合分子生物学和遗传学的研究成果,可以进一步揭示纺锤体在卵母细胞发育和受精过程中的作用机制。纺锤体的微管通过动态不稳定性来不断增长和缩短,从而牵引染色体运动。无损观察纺锤体卵冷冻研究
纺锤体在细胞分裂中的精确调控是生物体发育的基础。昆明克隆纺锤体透明带
在核移植过程中,纺锤体的稳定性是首要考虑的问题。冷冻和解冻过程中的温度变化和冷冻保护剂的毒性都可能对纺锤体造成损伤,导致染色体分离异常,进而影响胚胎发育。因此,如何在冷冻过程中保持纺锤体的稳定性,是核移植纺锤体卵冷冻研究面临的重要挑战。体细胞核在移入去核卵母细胞后,需要经历复杂的重新编程过程,以获得全能性。然而,这一过程受到多种因素的调控,包括表观遗传修饰、转录因子表达等。在冷冻过程中,这些调控机制可能受到干扰,导致重新编程失败或异常,从而影响胚胎发育。昆明克隆纺锤体透明带
- 北京DTS激光破膜ZILOS-TK 2025-05-19
- 上海双折射性纺锤体纺锤体结构 2025-05-19
- 北京ICSI纺锤体卵冷冻研究 2025-05-19
- 上海激光破膜 2025-05-19
- 上海自动打孔激光破膜辅助孵化 2025-05-19
- 香港DTS激光破膜胚胎干细胞 2025-05-19
- 香港无需染色纺锤体价格 2025-05-19
- 上海二极管激光激光破膜囊胚注射 2025-05-19
- 北京偏光成像纺锤体兼容大部分显微镜 2025-05-19
- 欧洲Hamilton Thorne激光破膜胚胎干细胞 2025-05-19
- 放心选信号隔离器GXGS2104 2025-05-19
- 江西安全阀哪里买 2025-05-19
- 激光切割钣金检测系统定制 2025-05-19
- 沈阳维氏硬度计价钱 2025-05-19
- 江苏流通池拜泰奇怎么样 2025-05-19
- 北京DTS激光破膜ZILOS-TK 2025-05-19
- 毛细管配件 2025-05-19
- 高灵敏度无转子流变仪供应商推荐 2025-05-19
- 宝山区如何选溢流阀保养 2025-05-19
- 测量工具实验室用品技术指导 2025-05-19