宁波抗体试剂进出口审批代办
在生物试剂进出口领域,法规政策起着关键的规范作用。不同国家和地区对生物试剂的进出口有着严格规定。例如,我国依据《中华人民共和国药品管理法》《医疗器械监督管理条例》等法规,对作为药品或医疗器械管理的生物试剂,要求企业具备相应资质,如药品经营许可证、医疗器械经营备案凭证等。对于一些特殊生物试剂,可能还涉及《生物制品批签发管理办法》,需取得批签发证明方可进口。美国食品药品监督管理局(FDA)对进口生物试剂也有详细准则,从产品注册、标签要求到生产质量管理规范(GMP)符合性审查等,确保产品安全有效。企业在开展进出口业务前,务必深入研究目标市场法规,完成各类许可申请与注册流程,避免因违规遭受处罚,影响业务开展。生物试剂进口申报文件必须真实有效,避免清关受阻。宁波抗体试剂进出口审批代办

生物试剂进出口企业,资质许可至关重要。进口企业需先完成对外贸易经营者备案登记,获取合法进出口权。若涉及药品类生物试剂进口,必须持有药品经营许可证,此证对仓储条件、人员资质等有严格要求,如仓库要分区域存储,且质量管理人员需有药学专业背景及从业经验。对于医疗器械类生物试剂,依据风险等级,低风险的需办理医疗器械经营备案凭证,中高风险的则要取得医疗器械经营许可证 。出口企业也得完成对外贸易经营者备案,生产企业还需持有相应的药品生产许可证或医疗器械生产许可证。此外,针对高风险生物制品或涉及两用物项的生物试剂,进出口都要提前申请特别许可,像生物制品批签发证明、两用物项和技术进出口许可证等。企业务必严格按规定流程申请,杜绝无证经营,否则将面临严重法律处罚,阻碍业务开展。苏州生物试剂出口前置审批代办生物试剂进口需提前规划好目的国境内的配送方案。

包装和标识在生物试剂进出口中举足轻重。包装材料要坚固耐用,且能适配试剂特性。强酸强碱类试剂要用耐腐蚀性包装,对光照敏感试剂需采用遮光包装,同时包装要具备良好密封性,防止泄漏。标识方面,必须清晰标注产品名称、成分、规格、生产企业、生产日期、有效期、储存条件、使用说明等信息。语言要符合目标市场要求,一般需用英语,在部分非英语国家,可能还得翻译成当地语言。对于危险生物试剂,要依据国际标准张贴危险货物标识,以此保障运输、储存和使用过程中的安全,避免因包装标识不当引发安全事故或通关受阻。
生物试剂进出口企业必须满足严格资质要求。在国内,从事生物试剂进出口的企业首先要具备合法的进出口经营权,需在商务部门完成对外贸易经营者备案登记。若涉及药品类生物试剂进出口,企业必须取得药品经营许可证,且其仓储、运输等条件要符合药品经营质量管理规范(GSP)。对于医疗器械类生物试剂,企业需进行医疗器械经营备案或取得医疗器械经营许可证,依据试剂风险等级而定。企业的人员资质也至关重要,要有熟悉生物试剂法规、质量控制和进出口业务流程的专业人员,如质量管理人员需具备相关专业背景及从业经验。此外,企业还需通过海关的信用评级,良好的信用等级有助于加快货物通关速度,保障进出口业务高效运行。出口生物试剂务必确保符合进口国严格的质量检测标准。
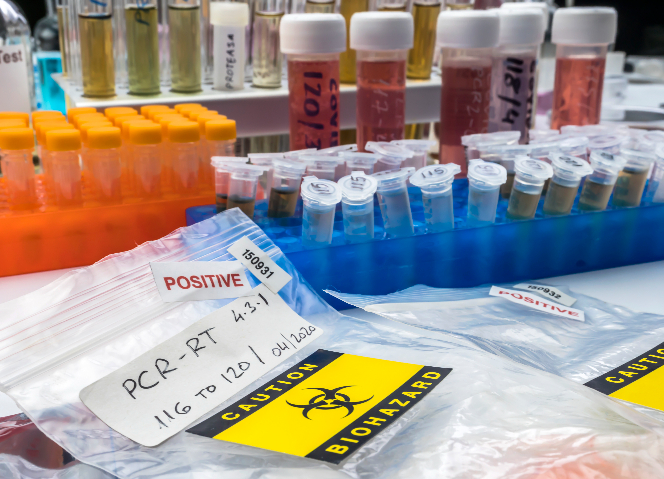
进出口的生物试剂必须符合目标市场的质量与安全标准。在出口环节,产品要多方面满足进口国法规及相关国际标准。以出口欧盟的生物试剂为例,其必须符合欧盟指令与协调标准,通过 CE 认证,该认证涵盖产品安全性、健康影响、环保等多方面评估,只有顺利通过认证机构检测与审核,获得认证证书,产品才能在欧盟市场流通。出口美国则要符合美国食品药品监督管理局(FDA)要求并完成相应注册程序,如医疗器械类生物试剂可能需进行 510 (k) 申请或上市前批准(PMA)等。进口生物试剂时,需确保其符合我国药品、医疗器械等相关法规,例如药品类生物试剂要符合我国药品注册标准,从药品的成分、纯度到稳定性等各方面都有细致规定;医疗器械类生物试剂要通过国内注册或备案,产品的研发、生产、质量控制等环节都要达到对应规范,否则产品将无法顺利通关,更无法进入市场销售,还可能面临召回、处罚等风险。出口生物试剂要确保产品在进口国的合法合规销售。杭州特殊物品进口前置审批代办
生物试剂进口申报时,需明确试剂的生物活性等级。宁波抗体试剂进出口审批代办
进境动植物源性生物试剂进口前,需向海关部门或出入境检验检疫机构申请检疫审批。企业需提交《进境动植物检疫许可证》申请表,说明试剂中动植物源性成分的来源国家或地区、用途、生产加工工艺、储存条件等信息。检疫部门会评估试剂携带病虫害、有害生物的风险,对于风险较高的试剂,可能要求企业提供额外的风险评估报告或采取特定检疫措施。审批通过后,企业获得《进境动植物检疫许可证》,凭证办理进口手续,防止外来有害生物通过生物试剂传入国内,维护生态平衡与农业安全。宁波抗体试剂进出口审批代办
- 南京保税区进口报关费用 2025-07-31
- 食品药品监管仓库一体化 2025-07-30
- 昆山细胞培养试剂进出口审批代办 2025-07-30
- 上海港生物试剂出口审批备案代办 2025-07-30
- 无锡核酸试剂进出口 2025-07-30
- 危险品监管仓储管理 2025-07-30
- 上海生物试剂出口审批单 2025-07-30
- 宁波细胞培养试剂进出口前置审批代办 2025-07-30
- 苏州特殊物品进口关税政策 2025-07-30
- 上海免疫诊断试剂进出口 2025-07-30
- 九江同城公路运输公司 2025-07-31
- 江苏到临沂货运配货 2025-07-31
- 湖北国内普通货运 2025-07-31
- 江西到美国海运DDP 2025-07-31
- 上海货物第三方物流运输服务业务 2025-07-31
- 常州电动画舫船价格 2025-07-31
- 杭州电商物流物流专线 2025-07-31
- 金华海外中转仓专线 2025-07-31
- 浦东新区短期小型仓储价格 2025-07-31
- 四轮车控制器价格 2025-07-31